Ⅰ. 서론
현대 의료에서 CT는 진단 및 치료에 있어 없어서는 안될 필수적인 도구로 자리잡아 가고 있다.1, 2, 3 암의 진단에서부터 각종 장기의 해부학적 형태 정보 등 CT를 통해 얻을 수 있는 정보는 매우 광범위하며,4, 5, 번호 그렇게 제공된 정보에 의해 의료의 질적 진보 또한 눈부신 발전을 이루어 가고 있다. CT의 기계적인 발전과 영상화 기술의 발달로 고화질 이미지에 익숙해 지면서 보다 양질의 이미지에 대한 요구 또한 점점 더 높아지고 있다. 하지만 고해상도 이미지 시대에 살고있는 우리의 눈높이에서 보자면 의료 영역에 제공되고 있는 CT 이미지는 아직까지는 부족하게 느껴지는 것이 현실이다.
연구실 영역에서 사용되고 있는 정밀 CT는 마이크로미터 단위를 넘어 나노미터를 바라보고 있다.7, 8, 9 이에 반해 의료용 CT는 사용되고 있는 장비의 수준에 비해 실제로 얻어지는 영상은 그 수준에 못 미치고 있다.10, 11, 12 의료용 CT가 가지는 한계점에는 여러가지 이유가 있겠지만, 사람을 직접 촬영해야 한다는 것이 가장 큰 이유일 거이다.13, 14, 15 사람은 연구실의 샘플들과 다르게 CT를 촬영하고 있는 그 순간에도 계속적으로 숨을 쉬며, CT를 촬영한다는 사실만으로도 긴장과 불안을 느끼며 미세한 떨림을 만들어 내게 된다. 이런 의도하지 않은 움직임들은 고스란히 CT 영상의 화질 저하로 이어지게 된다. 연구에 의하면 CBCT를 촬영하는 10-20 초 동안에도 환자는 약 2-10 mm의 폭으로 움직임 에러를 만든다고 한다.13 다시 말해 아무리 정밀한 기계를 가지고 CT 촬영을 하더라도 환자의 움직임이 만들어내는 에러를 수정하지 못한다면 1 mm 이상의 고해상도 화질을 가진 이미지를 선명하게 얻을 수 없게 된다. 더군다나 치과에서 가장 광범위하게 사용되고 있는 CBCT는 근사법(iterative method)을 사용해 이미지 보정 작업을 하게 되는데, CBCT의 에러 수정 과정의 복잡성으로 인해 아직 만족할 만한 결과를 보여주지 못하고 있다.16, 17 연구실에서 사용되는 평행광 CT(Parallel Beam CT, PBCT)는 비교적 작은 크기의 샘플을 대상으로 하고 샘플 자체의 움직임은 무시할 수 있는 상태로 CT 촬영을 하게 된다. 마이크로단위의 정밀도에서는 샘플 자체가 만들어내는 움직임 등에 대한 고려 보다는 기계적 정밀도를 높이는 것과 동시에, X-선을 이용하면서 발생하는 문제나 회전을 필요로 하는 촬영 환경에 의한 문제 등의 수정으로 촬영된 영상의 질을 높이는데 집중하였다.3, 18 하지만 정밀도가 나노미터 단위로 높아지면서 기계의 미세한 진동이나 촬영 과정에서 샘플의 미세한 움직임 등이 감지되면서 샘플의 움직임에 의한 에러가큰 문제로 대두되었으며 현재는 이를 해결하기 위한 연구가 활발히 진행되고 있다.19, 20 최근 Jun & Yoon 에 의해 제시된 VAM(Virtual Alignment Method)은21 샘플의 움직임에 의한 에러를 수정하는데 매우 의미 있는 결과를 보여주었다.
VAM은 샘플 내부 혹은 외부에 주변과 구분될 수 있는 방사선 투과도를 가진 영역인 특이점을 이용하게 된다. PBCT로 촬영된 투사영상의 모음인 사이노그램은 에러가 없는 상태에서는 특이점을 포함한 공간의 모든 위치들이 사인함수 곡선을 따르는 궤적을 보여준다. 하지만 CT를 촬영하는 동안 샘플의 움직임에 의한 에러가 발생하는 경우 사인함수 곡선에서 벗어나게 된다. 복잡한 사이노그램 상에서는 에러의 발생 유무 조차도 구분하기 힘들지만, 주변과 구분할 수 있는 특이점이 있는 경우에는 에러의 판별과 함께 특이점을 사인함수의 궤적을 따라가도록 수정함으로써 CT 촬영 중 발생한 샘플의 움직임에 의한 에러도 수정이 가능하다.21, 22, 23
팬텀 이미지(Phantom image)를 이용한 연구는 라돈 변환(Radon transform)과 라돈 역변환(Inverse Radon transform)을 이용하게 되는데, 이는 CT를 이용해 투사영상을 획득하고, 얻어진 투사영상을 통해 이미지를 재건하는 것과 동일한 과정이다.24, 25, 26 즉, 라돈 변환은 3차원의 이미지를 2차원의 이미지로 투사하는 과정으로 CT 촬영에서 투사영상을 얻는 과정과 동일한 과정으로 이해된다. 라돈 역변환은 라돈 변환으로 얻어진 각각의 투사 각도에 대한 이미지의 모음을 이용해 3차원 이미지로 재건하는 과정인데, 램퍼 필터 역투사(Ramper filter backprojection)을 사용해 재건할 수 있다.
본 연구에서는 사람의 치아와 유사한 팬텀 이미지를 이용하여 라돈 변환과 라돈 역변환 방식을 이용해 PBCT로 촬영한 상황을 재현한다. 여기에 CT가 촬영되는 동안 사람의 움직임 등에 의해 발생할 수 있는 에러를 부여하고 특이점과 VAM을 이용하여 수정함으로써, 치과영역에 PBCT의 적용 가능성을 타진하고자 한다.
Ⅱ. 재료 및 방법
특이점을 포함한 팬텀 이미지를 라돈 변환을 통해 투사영상 이미지를 만들고, 이렇게 얻어진 투사영상 이미지에 실제 임상에서 발생할 수 있는 에러를 부여한다. 에러를 포함한 투사영상의 사이노그램 (sinogram)은 형태적으로 Helgason-Ludwig Consistency Conditions(HLCC)를 만족하지 못한다.24 에러가 있는 사이노그램에서 특이점를 이용하여 에러를 수정하고 재건이미지를 얻는다.
1. 팬텀 이미지와 라돈 변환
2차원 팬텀 이미지를 이용한 라돈 변환은 PBCT에서 특정 축평면(axial plane)에 대한 투사영상을 얻는 것과 동일한 결과를 만들어 낼 수 있다(Fig. 1).25 본 연구에서는 팬텀이미지를 특정 축평면의 단면 형태로 가정하고 라돈 변환을 통해 사이노그램을 얻는데(Fig. 1), 0° - 180° 구간을 0.5° 간격으로 나누어 진행하였다. 라돈 변환을 시행할 이미지는 전체 50 × 50 픽셀이며, 각 픽셀의 크기는 20 µm로 가정하여 이미지의 크기는 10 mm × 10 mm 로 설정하였다. 사용된 팬텀 이미지는 치아와 유사한 형태를 가지도록 내부에 방사선 투과성이 높은 구조물이 존재하고 테두리에는 치아의 법랑질과 같은 방사선 불투과도가 높은 영역이 존재하도록 구성하였다. 더불어 특이점 역할을 할 영역을 팬텀 이미지의 표면에 삽입하였는데(Fig. 2A의 화살표), 이는 실제 치아 표면에 레진 태그를 부착하는 것과 유사한 상황을 고려하였다.
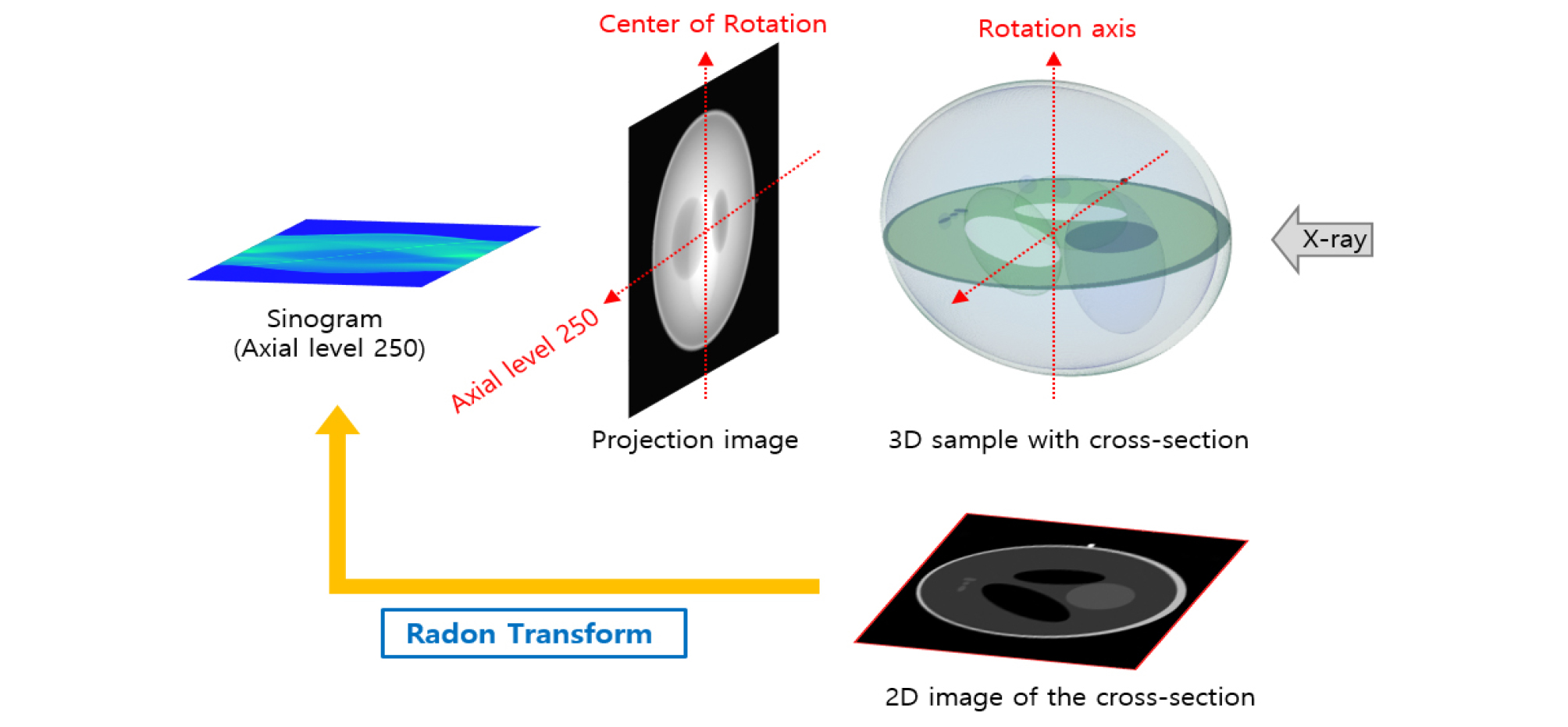
Fig. 1.
The projected image taken from CT scanning and the schematic diagrams of sinogram that was made with the projection information about the 3D sample's cross-sectioned area. The sinogram contains the information about 3D sample's cross-sectioned area. When the image of this area was Radon transformed, the same sinogram is obtained.
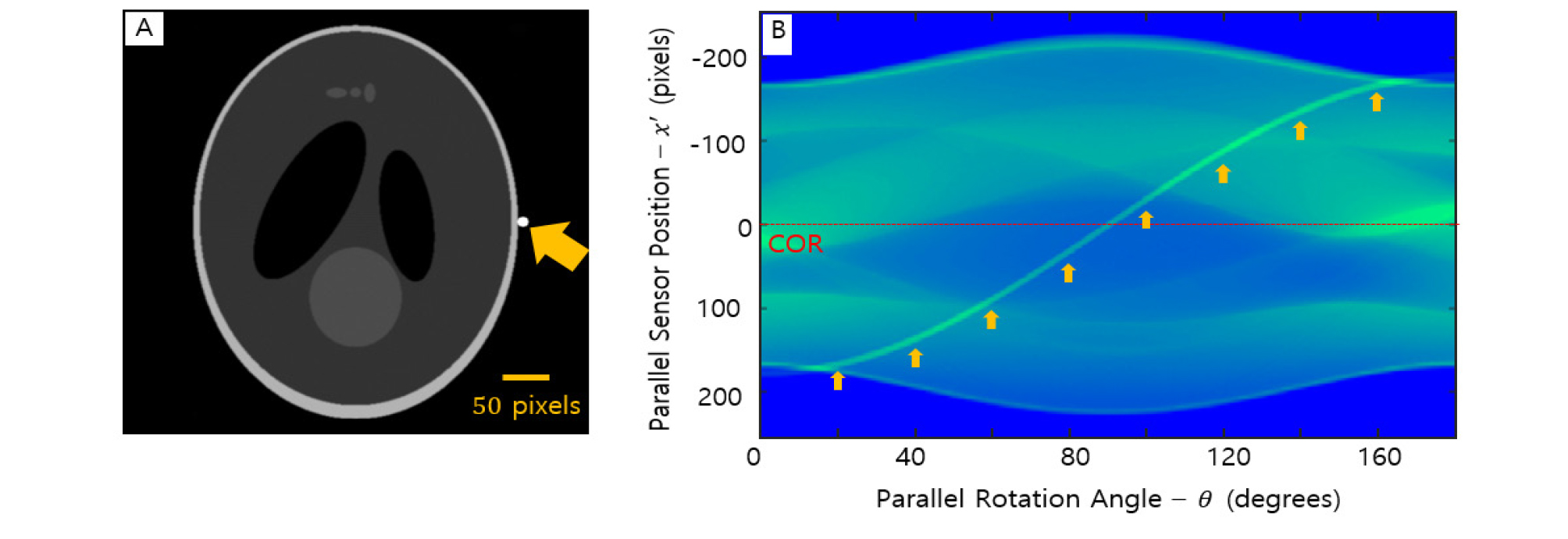
Fig. 2.
The phantom image and the sinogram. (A) The phantom image that resembles the shape of a tooth (the arrow shows the fixed point). (B) The sinogram that is obtained when the phantom image of (A) is Radon transformed. The line that cuts across the sinogram implies the center of rotation (the arrow shows the trajectory of the fixed point).
2. 에러 부여
CT 영상을 촬영하는 동안 발생할 수 있는 에러는 환자의 움직임에 의한 에러와 CT 기계가 돌아가면서 만들어내는 에러가 있다. 그 중 환자가 호흡 등으로 만들어내는 에러가 가장 큰 부분을 차지할 것으로 생각된다. 일반적으로 CT를 촬영하는 동안 환자의 움직임을 억제하기 위한 여러가지 기구와 방법들이 사용되는 점을 감안해 움직임의 폭은 최대 1 mm로 설정하였다.
CT가 촬영되는 시간 동안 총 6번의 호흡을 한 것으로 가정했다. 사람은 호흡을 통해 상하 진동 운동을 하게 되는데, 이로 인해 주기성을 가진 에러가 발생한다. 또한 환자는 CT를 촬영한다는 긴장감에 의해 조절할 수 없는 떨림이 발생할 수 있는데, 이 떨림은 어떤 주기성을 가지지 않고 전후좌우 무작위로 발생할 것이다. 따라서 본 연구에서는 상하로는 호흡에 의해 6회에 걸쳐 주기성을 가진 최대 1 mm(0.2, 0.4, 1 mm)의 폭을 가지는 오류를 부여하였고, 전후좌우로는 환자의 떨림에 의해 발생하는 무작위적인 움직임 에러를 최대 1 mm(0.2, 0.4, 1 mm)의 폭으로 부여하였다. X-선의 조사 방향과 같은 방향으로 움직임에러가 일어나는 경우 투사영상에서는 이미지의 변화가 없고, X-선의 조사 방향과 수직인 방향으로 움직임 에러가 일어나는 경우에는, 에러가 일어나는 방향을 따라 투사영상에서 이미지의 위치가 변한다.
3. 에러 수정
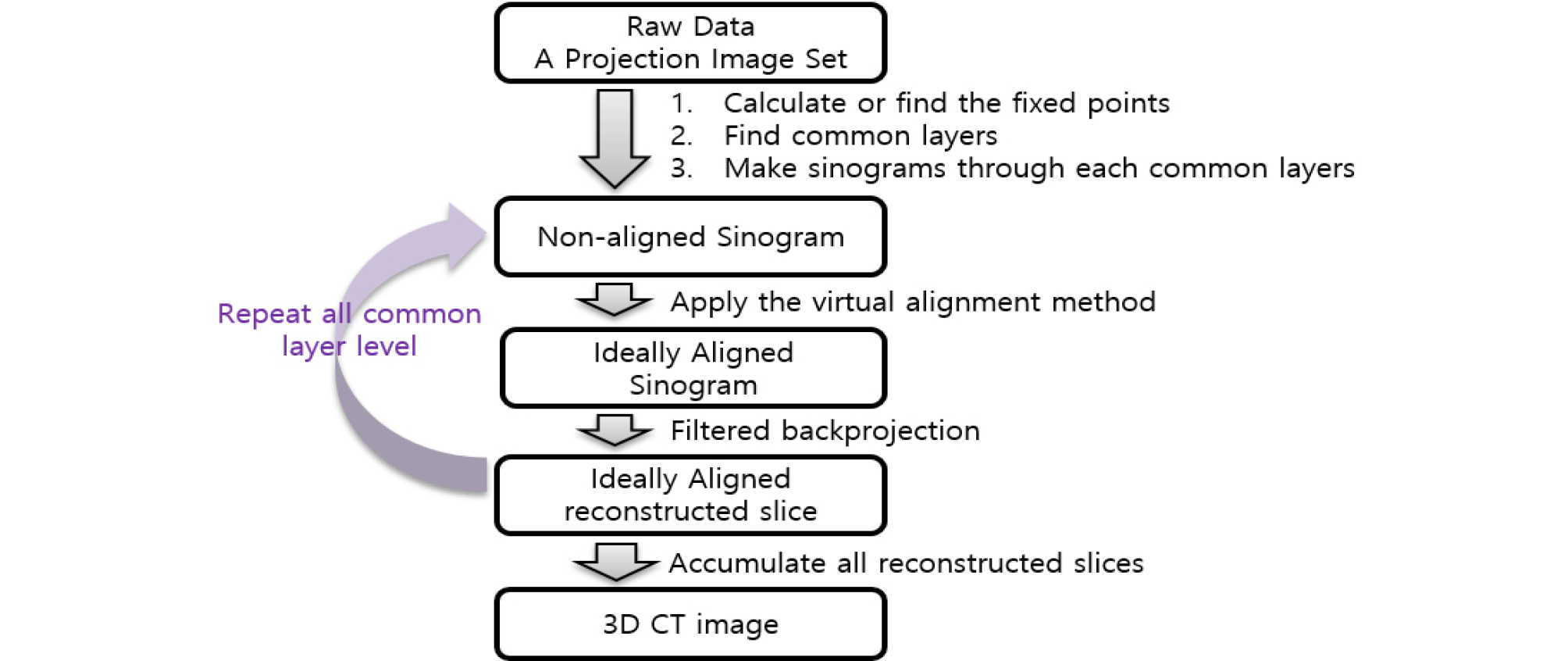
에러가 없는 이상적인 상황에서 PBCT가 촬영된 경우 촬영된 공간의 모든 위치들은 투사영상의 조합인 사이노그램에서 HLCC를 만족하는 패턴을 보인다. 바꾸어 말하면 사이노그램에서 특정 영역이 사인함수 곡선의 궤적을 벗어나 있다면 이는 에러가 있는 것이고, 이런 에러를 찾아 벗어난 궤적을 VAM 을 이용해 원래의 궤적으로 되돌려 줌으로서 에러를 수정할 수 있다. 본 연구에서는 이런 내용을 바탕으로 투사영상에서 구분할 수 있는 특이점을 설정하고 그 특이점을 기준으로 사이노그램을 수정한다. 보다 편리한 계산을 위해 특이점을 사이노그램 상의 중앙에 위치시켰는데, 이런 경우 특이점이 회전중심이 된다. 특이점을 사이노그램의 중앙으로 이동시킨 양 만큼 투사영상 이미지를 이동시키고 이미지 재건을 하면 에러가 수정된 재건이미지를 얻을 수 있다. 에러 수정 과정에 대한 모식도를 Fig. 3 에 나타내었다.
1) 얻어진 투사영상에서 특이점을 확인한다.
2) 하나의 축평면에 특이점이 놓일 수 있도록 투사영상의 상하 위치를 수정한다.
3) 특이점들이 놓여있는 특정 축평면의 사이노그램을 얻는다.
4) 사이노그램에서 촬영 각도에 따라 특이점들이 정상적인 사인함수 궤적을 그리도록 수정한다. 이때 특이점이 사이노그램의 중심에 오도록 수정하면 보다 간단한 계산이 가능하다.
5) 특이점이 사이노그램 상에서 정상적인 궤적을 그리도록 보정된 양 만큼 각각의 투사영상 이미지의 위치를 수정한 후 재건한다.
Ⅲ. 결과
본 연구에 사용된 팬텀 이미지를 이용한 라돈 변환 결과 특이점이 사인함수 곡선을 그리는 사이노그램을 얻을 수 있었다. Fig. 2B의 화살표가 특이점의 궤적의 위치를 나타내고 있다. 사이노그램의 중심을 가로지르는 지점에 표시한 선은 회전중심을 나타내며, CT 촬영 시 회전축에 해당하는 부분이다.
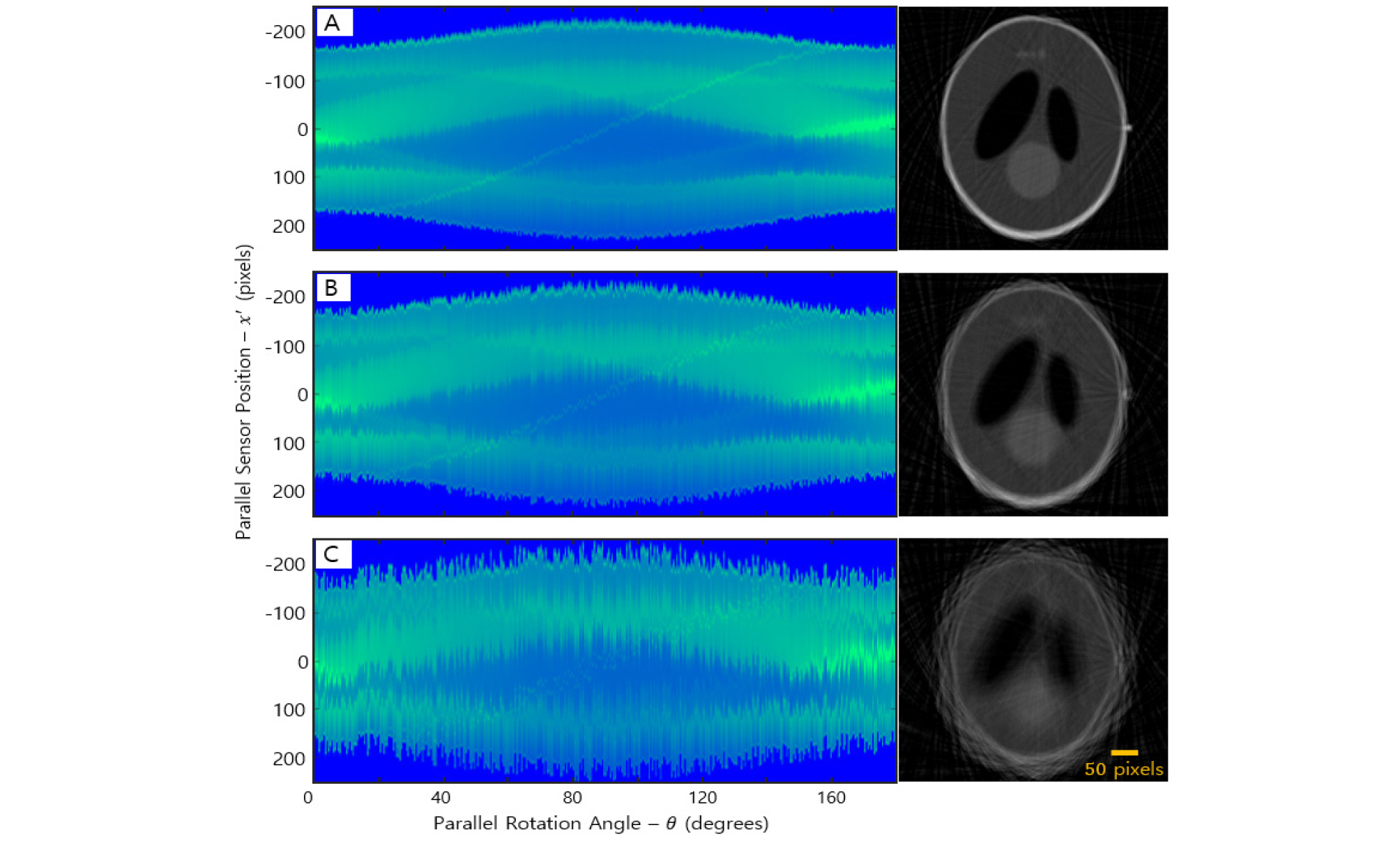
CT가 촬영되는 동안 환자의 움직임에 의해 발생할 수 있는 에러의 결과는 Fig. 4에 사이노그램과 재건이미지로 나타내었다. 상하 및 전후좌우 움직임의 폭은 사이노그램 기준으로 10, 20, 50개의 픽셀만큼 에러를 만들었고, 각 픽셀의 크기를 20 µm로 가정했기 때문에 실제 일어난 에러는 0.2, 0.4, 1 mm인 샘이다. 0.2 mm 의 에러 발생으로 사이노그램의 균질성이 상실되고 재건이미지에서 테두리의 변형이 관찰된다. 1 mm의 에러가 발생하는 경우 재건이미지 에서 구체적인 형태 뿐만 아니라 외형의 경계도 관찰하기 힘들다.
Fig. 2B의 사이노그램 전체를 가상의 더 넓은 공간의 중심에 오도록 수정한 것이 Fig. 5A이다. CT 촬영의 중심이 되는 회전축에 대해 수직 방향으로 공간을 확장한 것이다. 사이노그램 상에서는 위쪽과 아래쪽에 임의의 픽셀을 추가해 전체가 1,000개의 픽셀이 되도록 하였다. 사이노그램은 전체가 한덩어리로 위치만 이동하였고 사이노그램 내부의 궤적들은 그대로 유지하였다. 특이점의 궤적을 추적해 보면 기존과 동일한 사인함수 곡선을 그리고 있다.
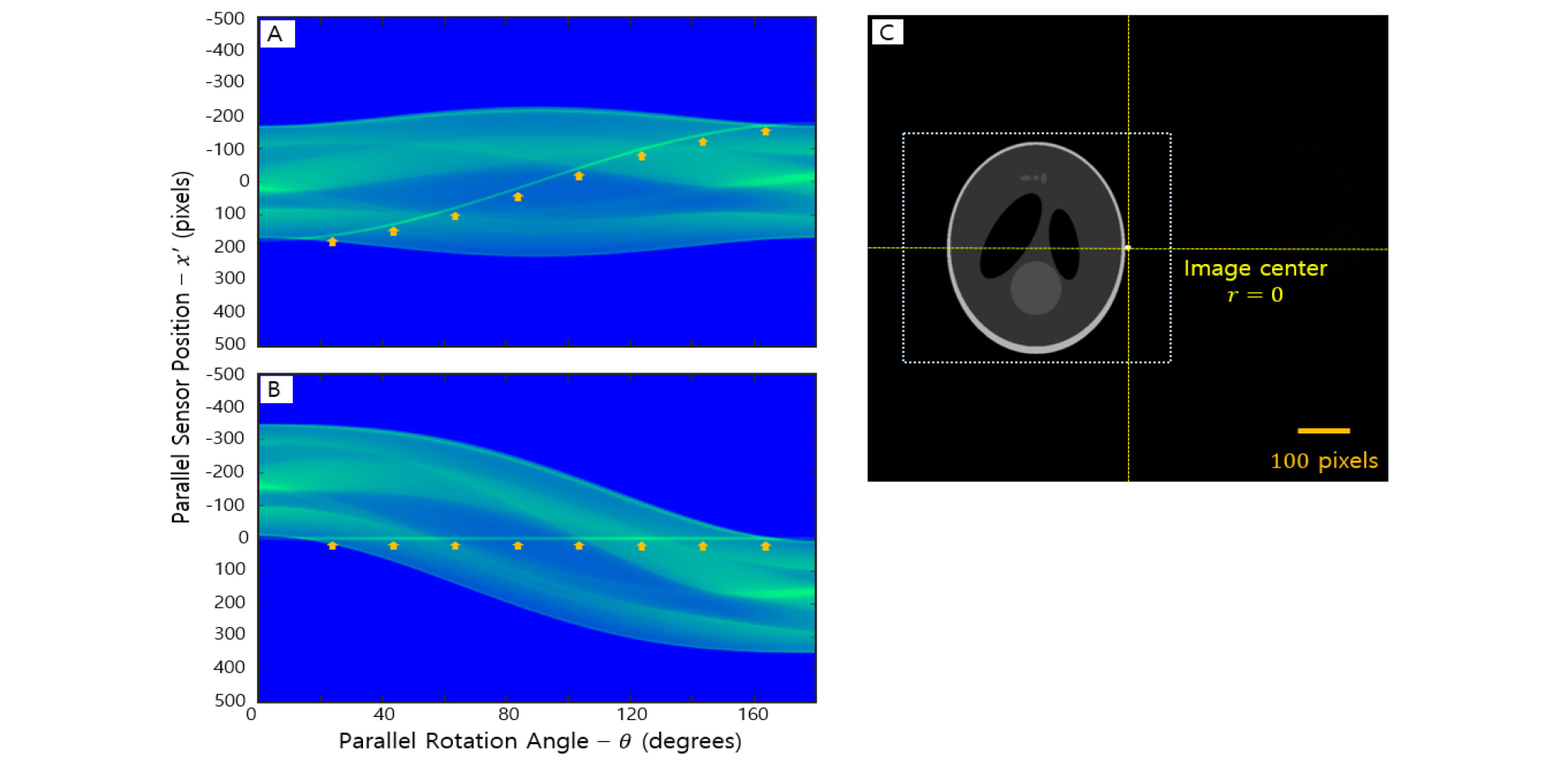
Fig. 5.
The sinograms and a reconstructed image that are expanded to a virtual space. (A) The sinogram with the original trajectory of the fixed point (the arrow shows the trajectory of the fixed point). (B) The sinogram in with the fixed point was moved to the center of rotation. The fixed point goes by the center of sinogram (the arrow shows the trajectory of the fixed point). (C) The reconstructed image where the fixed point is at the center of the whole image.
확장된 가상의 공간에 있는 팬텀 이미지를 수평 이동시켜 특이점이 회전축 상에 오도록 위치시킨다면, 특이점은 CT가 촬영되는 동안 위치 변화 없이 제자리에서 회전 만 할 것이다. 회전축 상에 특이점이 있으므로 그 궤적은 Fig. 5B에서 보듯이 사이노그램의 중심에 직선의 형태로 나타난다. 전체적인
사이노그램의 형태는 특이점의 위치를 변화시키기 전과는 많이 달라져 있으나 각각의 지점들의 흐름은 사인함수의 형태를 잘 따라가고 있다. Fig. 5C는 특이점을 회전중심으로 이동시킨 Fig. 5B의사이노그램을 이용해 라돈 역변환을 통해 재건한 이미지이다.
Ⅳ. 고찰
본 연구에서는 사람의 치아 형태를 닮은 팬텀 이미지를 이용해 PBCT 촬영 중 환자의 움직임 등에 의해 발생할 수 있는 에러를 VAM을 통해 수정함으로써, 치과영역에 PBCT의 적용 가능성을 보여주고자 하였다. VAM은 사이노그램 상에서 구분할 수 있는 특이점을 이용하게 되는데, Fig. 2A의 화살표로 표시한 부분과 같이 마치 치아 표면에 레진 태그를 부착한 것과 같은 상황을 고려해 방사선 불투과성이 높은 영역을 특이점으로 이용하였다. 이처럼 특이점은 사이노그램 상에서 그 궤적을 추적할 수만 있다면 적용이 가능하다.
어떤 특정 공간을 회전시키면서 그에 대한 투사영상을 획득하여 얻어지는 사이노그램은 에러가 없다면 모든 영역은 사인함수의 궤적을 그리게 된다. 그 궤도 함수 Tr,φ (θ) 는 아래와 같다.
Tr,φ (θ) = r×cos(θ-φ), 0° ≤ θ < 180°
여기서 r 은 회전 중심에서부터 특정 위치까지의 거리이다. θ 는 투사되는 X-선의 각도이고, φ 는 θ=0 일 때 투사되는 X-선과 회전중심에서부터 특이점의 연장선에 의해 형성되는 각도이다. 에러가 없는 한사이노그램의 중심은 회전중심이 되며 그 궤도함수는 r=0인 T0,φ (θ)=0 이고 직선의 형태로 나타난다. 우리가 특이점이라고 지정한 부분도 사이노그램에서 궤도함수를 따라야 한다. 때문에 사이노그램 상에서 특이점이 사인곡선을 그리지 않으면 사인곡선을 따라가도록 수정해주면 에러가 수정된다. 특이점의 위치에 따라 궤도함수의 진폭과 시작하는 위치만 달라진다. 회전중심에서 멀리 있으면 진폭이 커지고 가까이 있으면 진폭이 줄어든다. 만약 회전축 상에 특이점이 있다면 이 특이점은 진폭이 0이되고 사이노그램에서 한가운데 위치하게 된다. 특이점을 회전축 상에 오도록 하는 방법은 사이노그램에서 각각의 투사각도에서 얻어진 이미지를 이동시켜 특이점이 사이노그램의 중앙에 오도록 이동시키면 된다. 복잡한 계산이나 수식이 필요로 한 것이 아니라 중심에서 떨어진 거리만 알 수 있으면 우리는 언제나 특이점을 회전중심에 놓을 수 있는 것이다.
특이점을 회전중심으로 이동시키기 위해서는 우리의 시야를 CT 촬영을 통해 볼 수 있는 범위인 X-선 검출기의 크기에서 벗어나게 더 넓힐 필요가 있다. 특이점을 회전축 상으로 이동시키는 경우 사이노그램의 전체 형태가 처음의 직선 형태가 아닌 특이점을 중심으로 한 사인곡선 형태로 바뀌게 되는데(Fig. 5B) 이런 경우 기존의 500개의 픽셀에 한정해서 바라 보면 많은 양의 정보를 잃게 된다. VAM은 이런 문제를 가상의 공간에서 해결했다. 주어진 정보 영역에서 실제의 회전축이나 에러를 찾아 해결하려는 것이 아니라 특이점이 가상의 공간에서 중심에 오도록 공간 자체를 확장하는 것이다. 즉실제의 회전축을 사이노그램의 중심에 오도록 하는 것이 아닌 우리가 선택한 특이점이 사이노그램의 중심이 되도록 각각의 X-선 조사 각도에 해당하는 사이노그램의 상하 폭을 변화시키는 것이다. 이런 변화는 기존의 이미지에 화질이나 크기의 변화를 유발하지는 않는다. Fig. 5C와 Fig. 2A를 비교해 보면 팬텀 이미지를 둘러싼 주변 공간은 변화가 있으나 우리가 보고자 하는 이미지 자체는 왜곡이나 선명도의 차이가 관찰되지 않는다.
본 연구의 궁극적인 목표는 CT가 촬영되는 동안 발생하는 환자의 움직임 등에 의한 에러를 재촬영 없이 수정하고 주어진 환경에서 최대한의 선명한 이미지를 얻는데 있다. 하지만 아무리 정밀한 기계를 가지고 CT 촬영을 하더라도 Fig. 4에서 보인 것처럼 환자의 움직임이 1 mm 만 일어나도 촬영 대상의 내부 구조나 형태를 구분할 수 있는 정도는 많이 달라진다. 이런 이유가 PBCT를 의료 영역에 적용할 필요성을 못 느끼게 하지 않았을까 생각된다. 보다 저렴하고 사용하기 편한 CBCT 만으로도 PBCT로얻은 영상과 크게 다르지 않은 결과를 얻을 수 있다면 힘들게 PBCT를 의료 영역으로 받아들일 이유가 없는 것이다. 하지만 본 연구에서 제시하는 방법으로 PBCT의 화질을 기계적 한계점에 가깝게 끌어올릴수 있다면, 앞으로 PBCT에 대한 연구 방향은 많이 달라질 것으로 생각되며, 이런 연구의 축적이 의료 영역에 PBCT의 도입을 앞당길 것으로 기대된다. 이를 위해서는 사람의 치아 등을 이용해 실제 평행광 CT를 촬영한 데이터를 이용한 연구와 더 나아가 직접 사람을 대상으로 하는 연구, 그리고 현제는 연구실 영역에서만 활용 가능한 PBCT를 병원이나 의원 규모에서 사용할 수 있도록 하는 기계적인 연구 발전이 병행되어야 할 것이다.
치과영역에서 에러가 없는 양질의 CT 영상을 활용할 수 있게 된다면 보다 정확하고 정밀한 진단이 가능해 질 것이다. 이는 진료에 대한 확신과 함께 진료 효율성 향상에도 큰 기여를 할 수 있을 것이다. 예를 들어, 치아의 미세한 파절선 등에 대한 정확한 정보는 치아의 발치 여부를 판단해야 하는 치과의사에게 올바른 진단이 가능하도록 도움을 줄 수 있고, 불확실한 상태로 인해 환자가 겪게 될 수있는 고통을 줄여줄 것이다. 또한 치조골의 밀도나 형태 그리고 크기에 대한 신뢰성 있는 정보를 바탕으로 한 정확한 진단은 보다 정밀한 임플란트 식립 계획 수립과 그 계획에 대한 예지성 확보로 임플란트 치료의 질적 향상에 도움을 줄 것이다. 더불어 CAD/CAM을 활용한 보철물 제작 과정에서 치아에 대한 3차원 이미지를 CT를 통해 제공 받을 수 있다면 진단을 위한 CT 촬영에 머물지 않고 보철물의 제작과 같은 치료 영역으로의 확장된 활용도 가능할 것으로 생각된다. 이런 일련의 과정에서 보듯이 CT의 보다 효율적이고 발전된 활용은 치과 임플란트 치료의 진단에서부터 치료계획수립 그리고 최종적 보철물의 완성까지 전 과정에 걸쳐 많은 도움을 줄 것으로 기대된다.